凝乳酵素としてキモシン(レンネット)の他に植物由来の凝乳酵素(朝鮮アザミ)が知られています。最近、古くから日本や中国で食されている食用キノコ、ヤマブシタケ(学名:Hericium erinaceus)がβ-グルカンなど健康機能が知られている多糖類を含む他、凝乳活性もあることが報告されました(中村ら、食品科学工学会誌 61:444-447, 2014)。
ヤマブシタケで凝固させたチーズ(以後、Heチーズ)とキモシンで凝固させたチーズ(以後、Chチーズ)は何がどう違うのでしょうか。表1は両者の違いを比較したものです(谷本、佐藤、Milk Science 68: 100-105, 2019)。
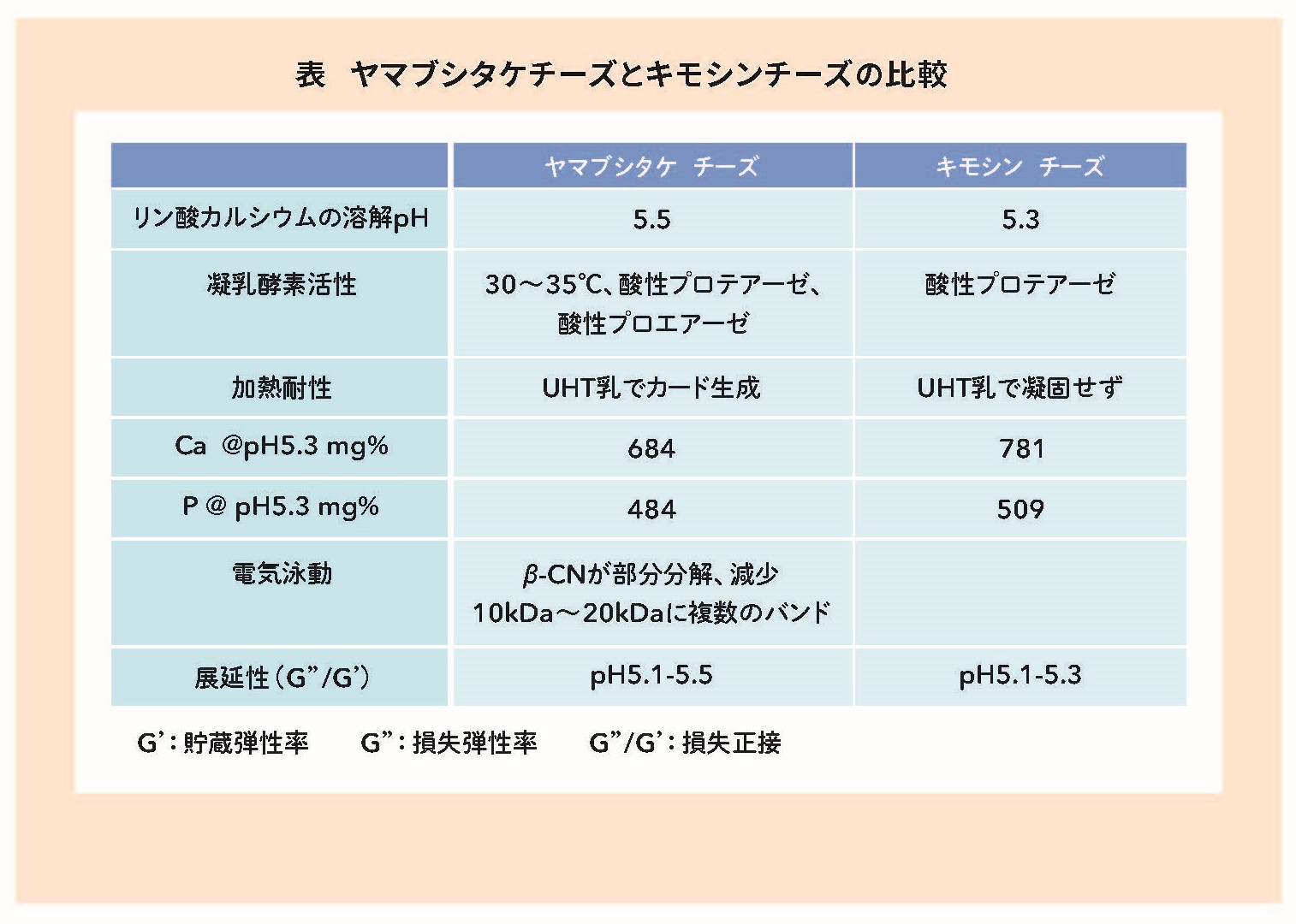
実用的な観点では、キモシンを使った場合、UHT殺菌乳ではカードを作れません。この理由については十分に解明されているわけではありませんが、加熱変性したホエイたんぱく質がカゼインミセルに結合することと関連していると考えられています。一方、ヤマブシタケを使った場合、UHT乳でもカードを得ることができます。この際、両チーズの電気泳動パターンには、ともにκ-カゼインの親水性ペプチドであるカゼインマクロペプチド(CMP:古くはGMPとも呼ばれていました)が生成し、カゼインミセルに残ったパラκ-カゼインのバンドをはっきりと検出することができます。すなわち、どちらの場合もκ-カゼインには凝乳酵素が働いているのです。
さらに、Chチーズに比べHeチーズはβ-カゼインのバンドが薄く、β-カゼインの一部が分解されています。そのせいか、Heチーズはやや苦味を感じると報告されています。Heチーズではヤマブシタケの粗抽出液に含まれているたんぱく質分解酵素がβ-カゼインを部分的に分解することで、カゼインミセルの性質がキモシン分解のそれとは異なっていることを示唆しています。
その結果、HeチーズではpH 5.5でリン酸カルシウムの多くがミセルからホエイに溶けだしています(図)。
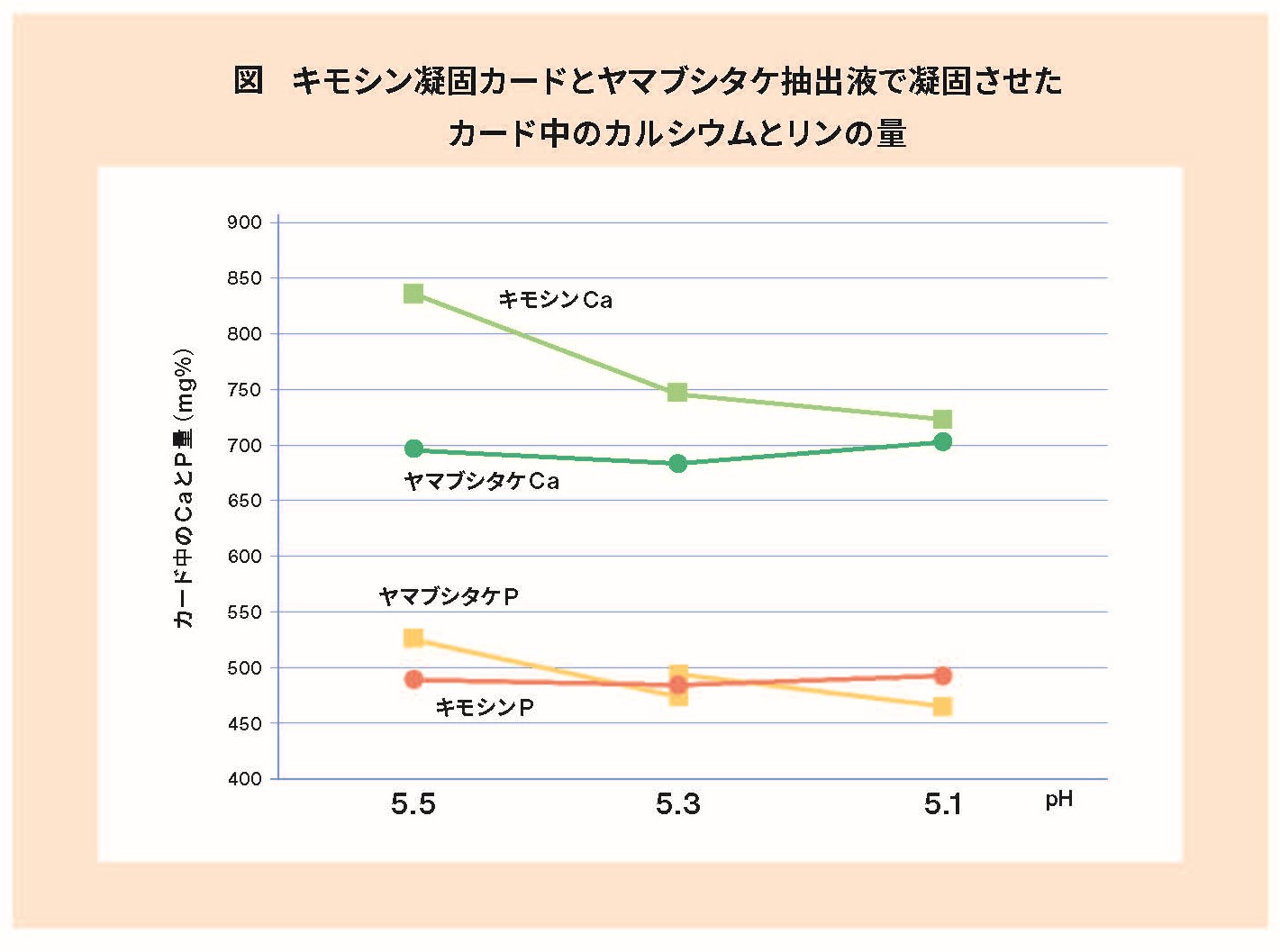
この理由も分かりません。ヤマブシタケ粗酵素によりミセルを構成しているβ-カゼインの一部が分解され、ミセル内部にあるリン酸カルシウムがミセル外部のホエイに触れやすくなった可能性もあり得ます。ヤマブシタケを用いたモッツァレラはpH5.5で、キモシンを使ったモッツァレラのpH5.1での展延性と同等の展延性を示します。なので、キモシンを使ったモッツァレラと同等の展延性が、ヤマブシタケを使ったモッツァレラではpH5.1~5.5の範囲で得られます。
このような研究結果は学術面でも興味深いものです。従来、カゼインミセルの安定性はκ-カゼインがミセル表面に分布しており、凝乳酵素によりκ-カゼインの親水性領域(CMP)が切断されることによりミセルが不安定になり凝固すると考えられてきました。高温加熱し、ホエイたんぱく質が結合するとκ-カゼインのCMPが切断されても、理由は定かではありませんが、凝固しなくなります。したがって、カゼインミセルの凝固や安定性にはκ-カゼインのみならず、β-カゼインも重要な役割を果たしていることが示唆されます。しかし、UHT加熱乳から得られるカードは低温殺菌乳から得られるカードに比べ軟弱でチーズにするにはイマイチだそうです。なので、Heチーズの実用化にはまだまだ時間がかかると思いますが、カゼインミセルの構造を考えるうえでは貴重な情報だと考えます。今後の進展が期待されます。
なお、この研究を手掛けられた谷本守正先生は本年2月に逝去されました。心よりご冥福をお祈りします。
「乳科学 マルド博士のミルク語り」は毎月20日に更新しています。
ⒸNPO法人チーズプロフェッショナル協会
無断転載禁
